МИНИ РЕВИЕВ
Испостава против рака: универзални маркери само за рак
Цхенгцхен Киан1, Ксиаолонг Зоу2, Веи Ли1,3, Иинсхан Ли4, Венкианг Иу5
1Схангхаи Епипробе Биотецхнологи Цо., Лтд, Шангај 200233, Кина;2 Одељење опште хирургије, Прва придружена болница Харбинског медицинског универзитета, Харбин 150001, Кина;3Схандонг Епипробе Медицал Лаборатори Цо., Лтд, Хезе 274108, Кина;4 Народна болница аутономног региона Нингкиа Хуи, Нингкиа Медицал Университи, Иинцхуан 750002, Кина;5 Шангајски клинички центар за јавно здравље и одељење за општу хирургију, болница Хуашан и институт за метастазе рака и лабораторија за епигенетику РНА, Институти биомедицинских наука, Шангајски медицински колеџ, Универзитет Фудан, Шангај 200032, Кина
АПСТРАКТАН
Рак је водећи узрок смрти широм света.Рано откривање рака може смањити смртност од свих врста рака;међутим, недостају ефикасни биомаркери за рано откривање за већину врста рака.Метилација ДНК је увек била главна мета интересовања јер се метилација ДНК обично дешава пре других генетских промена које се могу детектовати.Док се истражују уобичајене карактеристике рака помоћу новог водича за секвенцирање позиционирања за метилацију ДНК, серија универзалних маркера само за рак (УЦОМ) појавила се као јаки кандидати за ефикасно и тачно рано откривање рака.Док је клиничка вредност тренутних биомаркера рака умањена ниском осетљивошћу и/или ниском специфичношћу, јединствене карактеристике УЦОМ-а обезбеђују клинички значајне резултате.Валидација клиничког потенцијала УЦОМ-а код карцинома плућа, грлића материце, ендометријума и уротелија даље подржава примену УЦОМ-а у више врста карцинома и различитим клиничким сценаријима.У ствари, примене УЦОМ-а су тренутно под активном истрагом са даљом евалуацијом у раном откривању рака, помоћној дијагнози, ефикасности лечења и праћењу рецидива.Молекуларни механизми помоћу којих УЦОМ откривају рак су следеће важне теме које треба истражити.Примена УЦОМ-а у сценаријима из стварног света такође захтева имплементацију и усавршавање.
КЉУЧНЕ РЕЧИ
Откривање рака;скрининг рака;метилација ДНК;епигенетика рака;биомаркери рака
Зашто нам хитно треба ново биомаркери?
Након више од једног века борбе против рака, рак је и даље најсмртоноснија биолошка претња човечанству.Рак остаје глобални здравствени проблем са 19,3 милиона нових случајева и скоро 10 милиона смртних случајева процењених у 20201. Процењује се да је 2020. године у Кини дијагностиковано 4,6 милиона нових случајева рака, што чини 23,7% нових случајева рака у свету према ГЛОБОЦАН1.Штавише, око 3 милиона смртних случајева приписано је раку у Кини 2020. године, што је чинило 30% глобалних смртних случајева повезаних са раком1.Ове статистике су показале да је Кина на првом месту по учесталости и стопи смртности од рака.Штавише, петогодишња стопа преживљавања од рака је 40,5%, што је 1,5 пута ниже од петогодишње стопе преживљавања у Сједињеним Државама2,3.Релативно ниже преживљавање и веће стопе морталитета у Кини него у земљама са вишим индексима хуманог развоја сугеришу да је хитно потребан ефикасан и исплатив систем за превенцију и надзор рака.Рано откривање рака је један од најкритичнијих елемената у систему здравствене заштите.Рано откривање рака може побољшати прогнозу и преживљавање у раној фази код скоро свих типова рака4.Успешне стратегије скрининга довеле су до значајног пада инциденције и стопе морталитета од карцинома грлића материце, дојке, колоректалног карцинома и рака простате.
Међутим, није лак задатак да се постигне рано откривање рака.Истраживање биологије и прогнозе раног рака, идентификација и валидација поузданих биомаркера за рано откривање и развој приступачних и тачних технологија раног откривања су увек биле највеће препреке у том процесу4.Прецизно откривање рака може разликовати бенигне од малигних лезија, што помаже у избегавању непотребних процедура и олакшава даље управљање болестима.Тренутне стратегије раног откривања укључују биопсије засноване на ендоскопу, медицинско снимање, цитологију, имунотестове и тестове биомаркера5-7.Будући да су наметљиве и скупе, биопсије засноване на ендоскопу носе инхерентно тежак терет као главна медицинска процедура која се ослања на професионално особље.Као и цитологија, обе методе скрининга зависе од медицинских стручњака и засноване су на личном суду са учинком који је далеко од идеалног8.Насупрот томе, имунолошки тестови су веома нетачни, с обзиром на високу стопу лажно позитивних резултата.Медицинско снимање, као тактика скрининга, захтева скупу опрему и специјализоване техничаре.Стога је медицинско снимање изузетно ограничено због ниске приступачности.Из свих ових разлога, чини се да су биомаркери боља опција за рано откривање рака.
Преписка са: Иинсхан Ли и Венкианг Иу
Email: liyinshan@nxrmyy.com and wenqiangyu@fudan.edu.cn
ОРЦИД ИД: хттпс://орцид.орг/0009-0005-3340-6802 и
хттпс://орцид.орг/0000-0001-9920-1133
Примљено 22. августа 2023. године;прихваћено 12. октобра 2023. године;
објављено онлајн 28. новембра 2023.
Доступно на ввв.цанцербиомед.орг
©2023 Биологија и медицина рака.Цреативе Цоммонс
Аттрибутион-НонЦоммерциал 4.0 Интернатионал Лиценсе
Биомаркери су тренутно категорисани као протеини, маркери ДНК мутације, епигенетски маркери, хромозомске абнормалности, РНК маркери изведени директно из тумора или фрагменти тумора добијени индиректно из телесних течности.Протеински маркери су најшире примењени биомаркери у скринингу и дијагнози рака.Протеински биомаркери, као скрининг биомаркери, ограничени су тенденцијом да буду погођени бенигним лезијама, што доводи до претеране дијагнозе и претераног лечења, као што је пријављено за α-фетопротеин и простата-специфични антиген (ПСА)9,10.РНК маркери обухватају генетске обрасце експресије и друге некодирајуће РНК маркере. Комбинација генетичких експресионих РНК маркера може се открити коришћењем узорака урина, чија је осетљивост била далеко од задовољавајуће (60%) за примарне туморе, а детекција може на њих утиче природа лаке деградације РНК у нормалном окружењу11.И генетски и епигенетски маркери суочавају се са проблемом преваленције тумора и ограничења на типове рака.
Метилација ДНК је јак кандидат за биомаркер за рано откривање откако ју је Фајнберг први пут повезао са раком 1983. године12. Аберације метилације ДНК се примећују у свим стадијумима рака, већ у преканцерозном стадијуму.Аберантна хиперметилација ДНК се обично одвија на ЦпГ острвима у промоторима гена да би се супротставили супресорима тумора13,14.Студије су такође сугерисале да абнормална хиперметилација ДНК укључује регулацију развојних регулатора15.Долина метилације ДНК, која се обично повезује са регулаторима развоја и хиперметилованим карциномима, може пребацити начин експресије гена на стабилнији режим зависан од метилације ДНК и смањити везу са метилованим хистоном Х3К27ме3 и повезаним поликомб протеинима16,17.
Међу великим бројем објављених маркера метилације ДНК, неколико их је успешно дебитовало на тржишту;међутим, садашњи комерцијализовани маркери метилације ДНК и дијагностички панели тек треба да у потпуности откључају потенцијал раног откривања рака из више разлога18.Иако углавном показују прихватљиве перформансе користећи информације из базе података, ови биомаркери обично раде мање идеално у стварном свету због чињенице да су узорци из стварног света често сложенији и нису толико репрезентативни као они који су одабрани у базама података.Показало се да рано откривање метилације више карцинома засновано на секвенцирању има само 16,8% и 40,4% осетљивости у стадијуму рака И и ИИ, респективно19.Тестови за рано откривање захтевају већу стабилност и тачније биомаркере.
Откривање универзалног маркера само за рак (УЦОМ) помоћу секвенцирања водича за позиционирање (ГПС)
Упркос деценијама истраживања рака, задовољавајућа превенција и лечење нису реализовани.Потребне су нове методологије које би омогућиле истраживачима да темељно процене рак.Током последње 23 године, 6 обележја рака, као што су избегавање апоптозе, инвазија ткива и метастазе, итд., проширено је на 14 укључивањем карактеристика као што су немутационо епигенетичко репрограмирање и полиморфни микробиоми20,21.Како се открива више детаља који се тичу рака, више перспектива се уводи у истраживање рака.Истраживање рака постепено је постало новије у два правца (заједништво и индивидуалност).Са развојем прецизне онкологије последњих година, фокус истраживања рака се нагиње ка индивидуализованој циљаној терапији и хетерогености рака22.Стога су недавно идентификовани биомаркери рака фокусирани углавном на специфичне типове рака, као што су ПАКС6 форцервикални канцер23 и БМП3 за колоректални канцер24.Перформансе ових биомаркера специфичних за типове карцинома варирају, али још увек није могуће да се подложни појединци подвргну скринингу за све врсте рака истовремено због ограничења узимања биолошких узорака и високе цене.Било би идеално када бисмо могли да идентификујемо један, робустан биомаркер који је ефикасан за све врсте рака у раној фази.
Да би се постигао такав идеалан циљ, бољи кандидат за биомаркер мора бити изабран са листе потенцијалних типова биомаркера.Познато је да су аберације метилације ДНК, међу свим генетским и епигенетским профилима, повезане са раком и неке су од најранијих, ако не и првих, абнормалности повезаних са раком које се јављају хронолошки.Истрага о метилацији ДНК почела је рано, али је ометана недостатком истраживачких метода.Међу 28 милиона потенцијалних метилираних ЦпГ места у геному, број којим се може управљати мора бити откривен и усклађен са геномом да би се боље разумела туморигенеза.Секвенцирање бисулфита целог генома (ВГБС), које се сматра златним стандардом секвенцирања метилације ДНК, може покрити само 50% Цс у ћелијама рака због природе третмана бисулфитом који разбија фрагменте ДНК и смањује комплексност генома током трансформација Цс-у-Тс25.Друге методе, као што је 450к чипова, покривају само 1,6% метилације генома.На основу података од 450 хиљада, панел за детекцију метилације ДНК има осетљивост од 35,4% за 6 типова канцера у стадијуму И26.Ограничења типова рака, лоше перформансе и бука коју стварају методе детекције у аналитичком процесу постале су највеће препреке за панеле за откривање пан-карцинома.
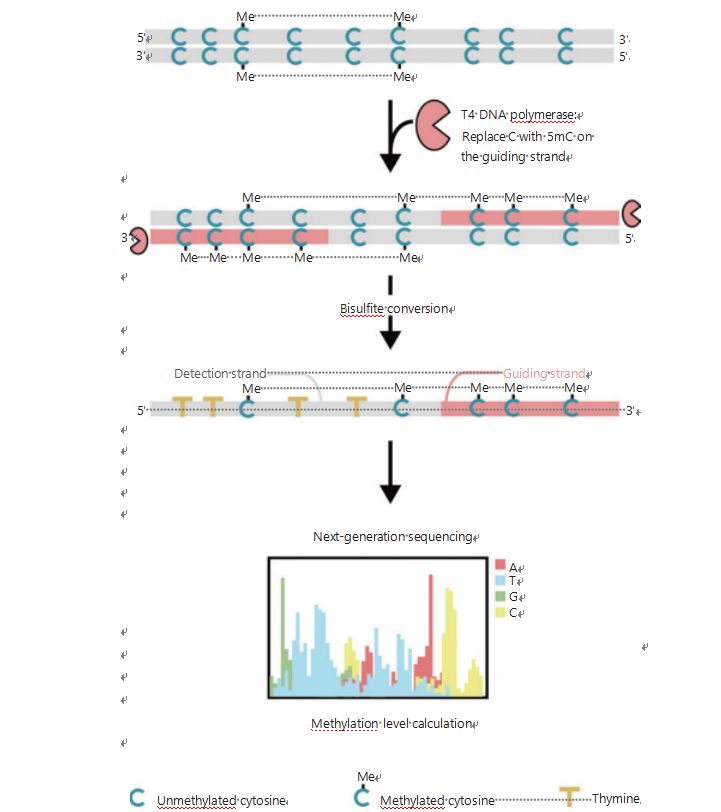
Да бисмо боље истражили епигенетске обрасце ћелија током туморигенезе и метастаза, развили смо јединствени ГПС за детекцију метилације ДНК у целом геному, који покрива до 96% ЦпГ места у 0,4 милијарде читања25.ГПС је метода билатералног секвенцирања која користи 3′ крај фрагмента ДНК неконвертибилних метил-цитозина након третмана бисулфитом који води рачунање поравнања ДНК метилације 5′ краја кроз секвенцирање у пару (Слика 1)25.Водећи ланац метил-цитозина, који делује као шаблонски ланац, помаже у усклађивању региона са високим ГЦ-ом које опоравља највише напуштене податке секвенцирања у традиционалном ВГБС.Карактеристика високе покривености ГПС-а пружа огромну количину информација о метилацији ДНК, што нам омогућава да испитамо профиле метилације рака са знатно већом резолуцијом у претходно недовољно истраживаним регионима.
ГПС нам пружа моћан алат за истраживање хомогености рака, који може у великој мери да поједностави истраживање рака и потенцијално пронађе универзално објашњење за туморигенезу и метастазе.Приликом анализе ГПС података о ћелијским линијама рака, често се сусрећемо са јединственим феноменом.Било је неколико региона за које се чинило да су абнормално хиперметилирани у више врста узорака рака.Овај неочекивани налаз је накнадно потврђен да служи као УЦОМ.Анализирано је више од 7.000 узорака из 17 типова рака у бази података Атлас генома рака (ТЦГА), међу којима смо идентификовали први УЦОМ, ХИСТ1Х4Ф, ген повезан са хистонима који је хиперметилиран у свим врстама рака27.Серија УЦОМ-а је затим пронађена и потврђена у бази података ТЦГА, бази података Гене Екпрессион Омнибус (ГЕО) и клиничким узорцима из стварног света.До сада су ХИСТ1Х4Ф, ПЦДХГБ7 и СИКС6 пронађени и потврђени као УЦОМ-и.Неочекивано откриће УЦОМ-а нуди моћан одговор на потребу за раним откривањем рака.УЦОМ-и пружају решење за детекцију вишеструких карцинома једним маркером.
Карактеристике УЦОМ-а
Након валидације, показало се да УЦОМ-и показују четири главне карактеристике које омогућавају УЦОМ-има да надмаше ефикасност тренутних биомаркера (Слика 2).
Јединствено за малигнитет
УЦОМ-и су јединствени за канцерозне или преканцерозне лезије и на њих не утичу нормалне физиолошке промене.Неки од тренутних маркера везаних за рак који се широко примењују у раном откривању и/или скринингу довели су до претеране дијагнозе.Повишени нивои ПСА, клинички акредитованог алата за скрининг, такође се откривају код бенигних стања, као што су хиперплазија простате и простатитис10.Прекомерна дијагноза и претерано лечење доводе до смањеног квалитета живота услед цревних, уринарних и сексуалних компликација28.Други биомаркери засновани на протеинима и широко коришћени у клиничком окружењу, као што је ЦА-125, нису дали значајне користи док су имали претерану дијагнозу и прекомерно лечење29.Висока специфичност УЦОМ-а за малигне болести избегава ове недостатке.УЦОМ, ПЦДХГБ7, ефикасно разликује сквамозне интраепителне лезије високог степена (ХСИЛ) и рак грлића материце од нормалних узорака и сквамозних интраепителних лезија ниског степена (ЛСИЛ), док већина других биомаркера може само разликовати рак грлића материце од нормалних узорака30.Иако ПЦДХГБ7 не открива значајне разлике између нормалног ендометријума и хиперплазије ендометријума, откривене су значајне разлике између нормалног ендометријума и атипичне хиперплазије, а још веће разлике су откривене између нормалног ендометријума и рака ендометријума (ЕЦ) на основу ПЦДХГБ731.УЦОМ-и су јединствени за малигне лезије у базама података и клиничким узорцима.Из перспективе пацијента, јединствени УЦОМ-и смањују праг за разумевање комплексних индикација различитих нестабилних биомаркера лошег учинка и одговарајуће анксиозности током процеса евалуације.Из перспективе клиничара, јединствени УЦОМ-и разликују малигне од бенигних лезија, што помаже у тријажи пацијената и смањује непотребне медицинске процедуре и прекомерно лечење.Стога, јединствени УЦОМ-и смањују редундантност медицинског система, олакшавају системски проблем и стављају на располагање више медицинских ресурса онима којима је потребно.
Слика 1 Шема ГПС тока рада за детекцију метилације ДНК25.Сива линија: улазна ДНК секвенца;црвена линија: ДНК третирана Т4 ДНК полимеразом, замењујући цитозин са 5′-метилцитозином на 3′ крају улаза;плави Ц са Ме: метиловани цитозин;плави Ц: неметиловани цитозин;жути Т: тимин25.
Све или ништа
УЦОМ су присутни само у ћелијама рака и стабилно се детектују у скоро свим ћелијама рака.Потврђено је да је ХИСТ1Х4Ф хиперметилиран у скоро свим типовима тумора, али не и у нормалним узорцима27.Слично, показало се да су ПЦДХГБ7 и СИКС6 хиперметиловани у свим узорцима тумора, али не и у нормалним узорцима30-32.Ова јединствена карактеристика значајно побољшава перформансе УЦОМ-а у погледу границе детекције и осетљивости.Само 2% ћелија рака може се разликовати у узорцима, што УЦОМ чини много осетљивијим биомаркером од већине постојећих биомаркера30. Као биомаркер који се користи за откривање колоректалног карцинома, КРАС мутације постоје само у приближно 36% случајева колоректалног карцинома, што указује на лош дијагностички потенцијал33.Ниска преваленција КРАС мутација код колоректалног карцинома ограничава КРАС у комбинацији са другим биомаркерима.У ствари, комбинација биомаркера у почетку може изгледати обећавајуће, али не даје увек задовољавајући резултат док показује много већи шум у анализи детекције и обично укључује компликованије експерименталне процедуре.Насупрот томе, ПЦДХГБ7 и други УЦОМ постоје код свих карцинома.УЦОМ-ови детектују канцерогене компоненте у различитим типовима узорака рака са највећом прецизношћу док искорењују сложене процесе анализе за поништавање буке.Није тешко открити рак у великом узорку, али је изузетно изазовно открити рак у малом узорку.УЦОМ-и су способни да открију мале количине рака.
Слика 2 Карактеристике УЦОМ-а.
Откривање карцинома који претходи патолошким променама
УЦОМ се могу открити у преканцерозном стадијуму пре патолошких промена.Као епигенетски биомаркери, УЦОМ абнормалности се јављају у ранијој фази од фенотипских абнормалности и могу се открити током туморигенезе, прогресије и метастаза34,35.Осетљивост УЦОМ-а током времена побољшава перформансе УЦОМ-а у откривању рака у раној фази и предканцерозних лезија.Откривање раног рака на основу биопсија и цитологије може бити тешко чак и за најискусније патологе.Једна биопсија добијена колпоскопијом је пријављена као позитивна у 60,6% ХСИЛ+ узорака.Потребне су додатне биопсије за вишеструке лезије да би се повећала осетљивост36.Насупрот томе, УЦОМ, ПЦДХГБ7, има осетљивост од 82% за ХСИЛ+ узорке, надмашујући осетљивост биопсија и већине биомаркера30.Маркер метилације, ФАМ19А4, има осетљивост од 69% за ЦИН2+, што је слично цитологији, али не може разликовати ЦИН1 од нормалних узорака37.Показало се да су УЦОМ-и много осетљивији биомаркер за рано откривање.У поређењу са патолозима заснованим на искуству, УЦОМ-и имају супериорну осетљивост на откривање карцинома у раној фази, што заузврат доприноси побољшању прогнозе рака и преживљавању30.Поред тога, УЦОМ-ови нуде платформу за детекцију која је доступна областима у којима недостају искусни патолози и увелико побољшава ефикасност детекције.Уз једнообразне процедуре узорковања и детекције, УЦОМ детекција даје стабилне и лако интерпретативне резултате који боље одговарају протоколу скрининга који захтева мање стручног особља и медицинских ресурса.
Лако се детектује
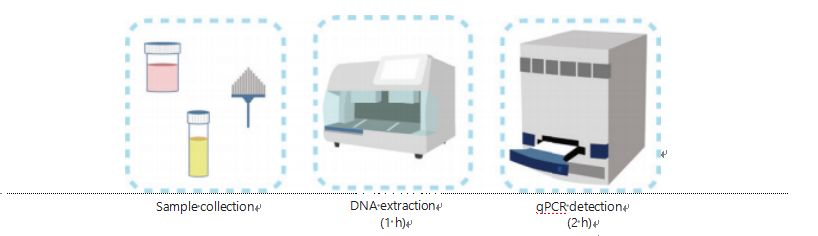
Тренутне методе за детекцију метилације ДНК су компликоване и дуготрајне.Већина метода захтева трансформацију бисулфита, што доводи до губитка квалитета узорка и могуће је да даје нестабилне и нетачне резултате.Лоша поновљивост узрокована третманом бисулфитом потенцијално доводи до конфузије за лекаре и пацијенте и додатно омета праћење и/или стратегије лечења.Због тога смо додатно модификовали метод детекције УЦОМ-а да бисмо избегли проблематичну обраду узорака бисулфитом, прилагодили захтевима клиничке примене и побољшали доступност.Развили смо нову методу користећи рестрикцијске ензиме осетљиве на метилацију у комбинацији са флуоресцентним квантитативним ПЦР-ом у реалном времену (Ме-кПЦР) да бисмо квантификовали статус метилације УЦОМ-а у року од 3 х коришћењем лаких процедура за руковање (слика 3).Ме-кПЦР може да прихвати више типова узорака, као што је клиничко сакупљање телесних течности и узорци урина који су сами прикупљени.Прикупљени клинички узорци се могу обрадити, ускладиштити и лако наставити са откривањем коришћењем стандардизоване и аутоматизоване екстракције ДНК.Екстрахована ДНК се затим може директно применити на Ме-кПЦР платформу за реакцију у једном лонцу и резултате квантификације излаза.Након једноставне анализе резултата коришћењем дијагностичких модела прилагођених и валидираних за специфичне типове рака, коначно одређивање резултата УЦОМ детекције се тумачи и представља као полуквантитативна вредност.Ме-кПЦР платформа надмашује традиционално бисулфитно-пиросеквенцију у детекцији УЦОМ-а док штеди 3 х конверзије бисулфита, према протоколу ЕЗ ДНК Метхилатион-Голд кит.Иновативна платформа за детекцију метилације чини УЦОМ детекцију стабилнијом, прецизнијом и приступачнијом30.
Слика 3 Процес детекције УЦОМ-а.Типови узорака укључују професионално узорковани БАЛФ, Папа четкицу и/или самосакупљени урин.Процес екстракције ДНК може да се прилагоди аутоматском екстрактору, чији се производ може директно детектовати кПЦР-ом.
Примена УЦОМ-а
Рак плућа
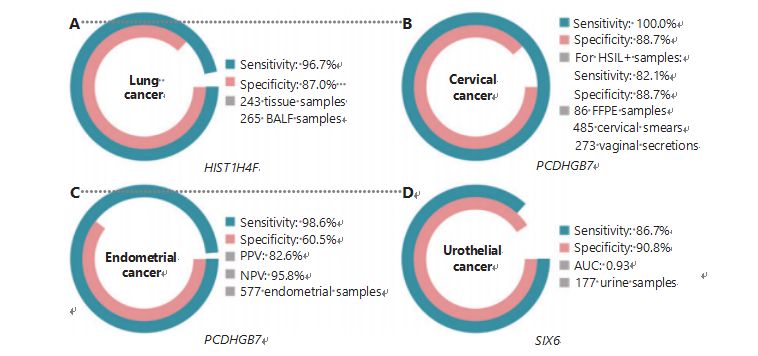
Рак плућа је други најчешће дијагностиковани и најсмртоноснији рак широм света, чинећи 11,4% нових случајева и 18,0% нових смртних случајева1.Међу свим дијагнозама, 85% је карцином немалих ћелија плућа (НСЦЛЦ), а 15% је карцином малих ћелија плућа (СЦЛЦ), који има виши ниво малигнитета38.Скенирање ниском дозом компјутеризоване томографије (ЛДЦТ) је тренутно препоручена метода скрининга за рак плућа и показало се да побољшава рано откривање и смањује смртност6;међутим, због ниске специфичности и лоше доступности, ЛДЦТ тек треба да послужи као задовољавајући метод скрининга, као и други уобичајени маркери рака, као што је ЦЕА39.Трошкови и потенцијал за промашене дијагнозе и погрешне дијагнозе стратегије ЛДЦТ скрининга ометају напредак промоције скрининга рака плућа40.ХИСТ1Х4Ф, УЦОМ, има огроман потенцијал као биомаркер за рано откривање у узорцима бронхоалвеоларне течности (БАЛФ)27.ХИСТ1Х4Ф је хиперметилован у аденокарциному плућа и карциному сквамозних ћелија плућа, са специфичношћу детекције од 96,7% и осетљивошћу од 87,0% (Слика 4А), и изузетним перформансама за стадијум И рака27.ХИСТ1Х4Ф има специфичност од 96,5% и осетљивост од 85,4% за НСЦЛЦ, и 96,5% и 95,7%, респективно, за СЦЛЦ27.Поред тога, узорци осам других типова карцинома, укључујући карцином панкреаса и колоректални карцином, потврдили су да је ХИСТ1Х4Ф хиперметилиран у свих осам типова27.
Рак грлића материце
Рак грлића материце је био четврти најчешће дијагностиковани рак и четврти водећи узрок смрти од рака код жена у 2020. години, чинећи 3,1% нових случајева и 3,4% смртних случајева повезаних са раком у свету1.Да би се елиминисао рак грлића материце до 2030. године, како је предложила СЗО, неопходно је рано откривање рака грлића материце.Ако се открије у раној фази, петогодишња стопа преживљавања достиже 92% код инвазивног карцинома грлића материце41.Смернице Америчког друштва за рак (АЦС) предлажу цитолошке тестове грлића материце, примарне ХПВ тестове или тестове за скрининг42.Цервикална цитологија је инвазивна и може открити само 63,5% случајева ЦИН2+37.
ПЦДХГБ7 је, насупрот томе, показао много боље резултате користећи Папа тестове и вагинални секрет, и може ефикасно разликовати ХСИЛ од ЛСИЛ у ултра-раној фази.Сам ПЦДХГБ7 има осетљивост од 100,0% и специфичност од 88,7% за рак грлића материце (Слика 4Б), и 82,1% осетљивост и 88,7% специфичност за ХСИЛ+ узорке30.ПЦДХГБ7 такође има 90,9% осетљивости и 90,4% специфичности у узорцима вагиналног секрета за рак грлића материце, које је много лакше прикупити30.Када се комбинује са високоризичним (хр)ХПВ тестом или Тхинпреп цитолошким тестом (ТЦТ), ПЦДХГБ7 има повећану осетљивост од 95,7% и специфичност од 96,2%, значајно надмашујући хрХПВ тест (20,3%), ТЦТ (51,2% ), и два комбинована (57,8%) за рак грлића материце30.Такође се показало да је ПЦДХГБ7 хиперметилиран у 17 типова рака из ТЦГА базе података, што указује на његову погодност у УЦОМ породици30.
Слика 4 УЦОМ-и су потврђени за четири типа рака у великим клиничким студијама.А. Учинак ХИСТ1Х4Ф, УЦОМ-а, у откривању рака плућа 508 узорака.Б. Учинак ПЦДХГБ7, УЦОМ, у откривању рака грлића материце 844 узорка.Ц. Перформансе ПЦДХГБ7, УЦОМ, у детекцији рака ендометријума 577 узорака Папа и Тао четкица ендометријума.Д. Перформансе СИКС6, УЦОМ-а, у детекцији рака уротела 177 узорака.
EC
ЕК је један од најчешћих карцинома женског репродуктивног система широм света, са процењеним 4,2 милиона нових случајева и 1% смртних случајева од рака годишње1.Уз успешну дијагнозу у раној фази, ЕЦ је излечив и има 5-годишњу стопу преживљавања од 95% за стадијум И рака.Пацијенти са симптомима, као што је абнормално крварење из материце, добијају периодичну клиничку процену и подвргавају се инвазивним и болним процедурама биопсије, упркос томе што само 5%–10% на крају развије ЕЦ43.Трансвагинални ултразвук, као уобичајена метода детекције, веома је непоуздан због своје неспособности да разликује бенигне од малигних промена ендометријума и високе стопе лажно позитивних44.
Урађено је паралелно поређење серумског ЦА-125, широко примењеног ЕЦ биомаркера, и ПЦДХГБ7.Серум ЦА-125 је имао осетљивост од 24,8%, што сугерише да је ЦА-125 неадекватан маркер за ЕЦ упркос специфичности од 92,3%31.Детекција ПЦДХГБ7 помоћу узорака Пап четкица дала је осетљивост од 80,65% и специфичност од 82,81% за ЕЦаталл фазе, док је Тао четкица имала осетљивост од 61,29% и специфичност од 95,31%31.ПЦДХГБ7 дијагностички модел, заснован на Ме-кПЦР, дао је осетљивост од 98,61%, специфичност од 60,5% и укупну тачност од 85,5%, користећи узорке Пап и Тао четкице (Слика 4Ц)31.
Уротелни рак
Уротелни карцином, који се састоји од карцинома бешике, бубрежне карлице и уретера, био је седми најчешће дијагностиковани карцином у 2020. години широм света, узрокујући 5,2% нових случајева и 3,9% смртних случајева1.Уротелни карциноми, од којих је више од 50% рак мокраћне бешике, били су четврти најчешће дијагностиковани рак у Сједињеним Државама 2022. године, чинећи 11,6% новодијагностикованих случајева3.Приближно 75% карцинома мокраћне бешике је класификовано као немишићно инвазивни канцер мокраћне бешике ограничен на мукозу или субмукозу45.Биопсија цистоскопије је златни стандард за дијагностиковање уротелног карцинома који се спроводи флуоресцентном ин ситу хибридизацијом (ФИСХ) и цитолошким тестовима.ФИСХ и цитологија имају лоше дијагностичке перформансе, а цистоскопија је интрузивна и има основни ризик од пропуштања микролезија, погрешног тумачења лезија и потенцијалног изазивања ширења или рецидива рака46.Претходно валидирани УЦОМ, ПЦДХГБ7, такође се показао као хиперметилиран код уротелног карцинома, са површином испод криве од 0,86, што указује на потенцијалну дијагностичку способност30.Да би се додатно потврдило више УЦОМ-а и боље прилагодило више типова узорака, СИКС6, нови УЦОМ, је испитан и показао одличан дијагностички потенцијал у раном откривању уротелног карцинома коришћењем узорака урина на Ме-кПЦР платформи.Детекција СИКС6 помоћу узорака урина показала је компетитивну осетљивост од 86,7% и специфичност од 90,8% (слика 4Д), док је била неинвазивна и лака за преузимање32.Тренутно се истражује потенцијал СИКС6 у праћењу метастаза и процени ефикасности лечења.
Будућност и изазови
УЦОМ-и имају јак учинак у дијагностичком потенцијалу вишеструких карцинома, али има још много посла да се уради.Проширили смо листу УЦОМ-а и активно смо проверавали УЦОМ-е у више врста рака, укључујући и оне које је традиционално тешко открити.Резултати валидације из ТЦГА база података додатно су потврдили примену УЦОМ-а у више врста рака и у више ситуација.У прелиминарном истраживању, показало се да УЦОМ-и имају снажан дијагностички потенцијал за холангиокарциноме и аденокарциноме панкреаса, које је скоро немогуће дијагностиковати у раној фази тренутним методама скрининга32,47.Способност откривања ретких карцинома помоћу УЦОМ-а може се користити са циркулишућом ДНК тумора (цтДНК) помоћу побољшане платформе за течну биопсију48.Студија која је укључивала панел за откривање пан-карцинома заснованог на ДНК плазме дала је осетљивост од 57,9%49.Упркос високој специфичности, свеукупни учинак открива да још има простора за побољшање.
Јединствене карактеристике УЦОМ-а су такође подржале истраживање потенцијала УЦОМ-а у процени ефикасности лечења и праћењу рецидива.Према Критеријумима за процену одговора код солидних тумора (РЕЦИСТ), медицинско снимање је препоручена методологија за праћење рецидива и процену ефикасности лечења, док се туморски маркери користе сами за процену50.У стварности, међутим, на приступе сликању у великој мери утичу учесталост и тајминг, и стога излажу пацијенте већем ризику и трошковима51,52.СИКС6 је потврђено да служи као предиктор за метастазе рака дојке32.Праћење цтДНК засновано на течној биопсији омогућава надзор у реалном времену над минималним резидуалним болестима месецима пре радиолошке детекције, идеално одлажући и спречавајући прогресију рака повезаног са рецидивом53.Прелиминарни резултати сугеришу да УЦОМ одражавају ниво канцерогене хиперметилације у реалном времену одмах након операције и лечења32.Висока осетљивост коју показују УЦОМ-и и применљивост у вишеструким неинтрузивним типовима узорака омогућавају УЦОМ-има да служе као прецизан биомаркер за праћење рецидива уз одржавање високе сагласности пацијената.
Истовремено, јавна доступност теста је још једно важно питање које захтева додатне напоре.Док је сарадња у откривању УЦОМ-а усвојена у више болница у нади да ће имати користи од већег броја пацијената, про боно детекције и скрининги се активно обављају у руралној Кини.УЦОМ-и захтевају побољшану доступност да би се квалификовали као изводљиво средство за скрининг, посебно за неразвијена подручја.
Док резултати апликације УЦОМ у раном откривању обећавају, постоје многе непознанице о УЦОМ-у.Уз активно истраживање, додатна истраживања су оправдана о томе зашто су УЦОМ-и универзално присутни код карцинома.Основни механизми епигенетске регулације који леже у основи УЦОМ-а су вредни даљег истраживања, што би могло оправдати нови правац за терапију рака.Враћајући се на интеракцију између хомогености тумора и хетерогености, занима нас зашто УЦОМ-и могу бити изузетак од већине биомаркера рака који су уско повезани са специфичним типовима рака.Улога аберација метилације ДНК идентификованих УЦОМ-ом у туморигенези, прогресији тумора и метастазама није утврђена у процесу губитка и враћања ћелијског идентитета и захтева детаљну инспекцију.Други велики интерес лежи у обиму инкорпорације особине хомогености УЦОМ-а са ткивним јединственим маркерима у нади да ће се приближити прецизном откривању трагова рака и идентификацији порекла туморског ткива на обрнути начин.УЦОМ-и могу бити идеално средство за превенцију рака, откривање рака и потенцијалну одбрану и уклањање рака.
Грант суппорт
Овај рад је подржан од стране Националног кључног програма за истраживање и развој Кине (Грант бр. 2022БЕГ01003), Националне фондације за природне науке Кине (бр. грантова 32270645 и 32000505), гранта од стране здравствене комисије провинције Хеилонгјианг (грант бр. 2020-111) , и грант од Хезе Института за науку и технологију (Грант бр. 2021КЈПТ07).
Изјава о сукобу интереса
Веи Ли је директор истраживања и развоја за Схангхаи Епипробе Биотецхнологи Цо., Лтд. Венкианг Иу је члан Научног саветодавног одбора Епипробе-а.В. Иу и Епипробе су одобрили патенте на чекању у вези са овим радом.Сви остали аутори изјављују да немају супротстављене интересе.
Прилози аутора
Осмислили и дизајнирали пројекат: Цхенгцхен Киан и Венкианг Иу.
Написао је рад: Цхенгцхен Киан.
Направио илустрације: Цхенгцхен Киан.
Рецензирао и уредио рукопис: Ксиаолонг Зоу, Веи Ли, Иинсхан Ли и Венкианг Иу.
Референце
1. Сунг Х, Ферлаи Ј, Сиегел РЛ, ЛаверсаннеМ, Соерјоматарам И, Јемал А, ет ал.Глобална статистика рака 2020: ГЛОБОЦАН процене од
инциденција и морталитет широм света за 36 карцинома у 185 земаља.ЦА Цанцер Ј Цлин.2021;71: 209-49.
2. Ксиа Ц, Донг Кс, Ли Х, Цао М, Сун Д, Хе С, ет ал.Статистика рака у Кини и Сједињеним Државама, 2022: профили, трендови и детерминанте.Цхин МедЈ (Енгл).2022;135: 584-90.
3. Сиегел РЛ, Миллер КД, ВаглеНС, ЈемалА.Статистика рака, 2023. ЦА Цанцер Ј Цлин.2023;73: 17-48.
4. Цросби Д, БхатиаС, Бриндле КМ, Цоуссенс ЛМ, Диве Ц, Ембертон М, ет ал.Рано откривање рака.Наука.2022;375: еааи9040.
5. Ладабаум У, Доминитз ЈА, КахиЦ, Сцхоен РЕ.Стратегије за
скрининг рака дебелог црева.Гастроентерологија.2020;158: 418-32.
6. Таноуе ЛТ, Таннер НТ, Гоулд МК, Силвестри ГА.Скрининг рака плућа.Ам Ј Респир Црит Царе Мед.2015;191: 19-33.
7. Боувард В, ВентзенсенН, Мацкие А, Беркхоф Ј, БротхертонЈ, Гиорги-Росси П, ет ал.Перспектива ИАРЦ-а на скрининг рака грлића материце.Н ЕнглЈ Мед.2021;385: 1908-18.
8. Ксуе П, Нг МТА, КиаоИ.Изазови колпоскопије за скрининг рака грлића материце у ЛМИЦ-има и решења вештачке интелигенције.БМЦ Мед.2020;18: 169.
9. Јохнсон П, Зхоу К, Дао ДИ, Ло ИМД.Циркулишући биомаркери у дијагнози и лечењу хепатоцелуларног карцинома.Нат Рев Гастроентерол Хепатол.2022;19: 670-81.
10. Ван ПоппелХ, Албрехт Т, Басу П, ХогенхоутР, ЦолленС, Рообол М. Рано откривање рака простате засновано на серуму ПСА у Европи и глобално: прошлост, садашњост и будућност.Нат Рев Урол.2022;19:
562-72.
11. ХолиоакеА, О'Сулливан П, Поллоцк Р, Бест Т, Ватанабе Ј, КајитаИ,
ет ал.Развој мултиплекс РНК теста урина за детекцију и стратификацију карцинома прелазних ћелија бешике.Цлин Цанцер Рес.2008;14: 742-9.
12. Феинберг АП, Вогелстеин Б. Хипометилација разликује гене неких карцинома код људи од њихових нормалних колега.Природа.1983;301: 89-92.
13. Нг ЈМ, Иу Ј. Хиперметилација тумора супресорских гена као потенцијални биомаркери у колоректалном карциному.ИнтЈ Мол Сци.2015;16: 2472-96.
14. Естеллер М. Епигеномика рака: ДНК метиломи и мапе модификације хистона.Нат Рев Генет.2007;8: 286-98.
15. Нисхииама А, Наканисхи М. Навигација кроз пејзаж метилације ДНК рака.Трендс Генет.2021;37: 1012-27.
16. Ксие В, Сцхултз МД, ЛистерР, Хоу З, Рајагопал Н, Раи П, ет ал.Епигеномска анализа вишелинијске диференцијације људских ембрионалних матичних ћелија.Ћелија.2013;153: 1134-48.
17. Ли И, Зхенг Х, Ванг К, Зхоу Ц, ВеиЛ, Лиу Кс, ет ал.Анализе широм генома откривају улогу Полицомба у промовисању хипометилације долина метилације ДНК.Геноме Биол.2018;19: 18.
18. Коцх А, ЈоостенСЦ, Фенг З, де Руијтер ТЦ, ДрахтМКС, МелоттеВ,
ет ал.Анализа метилације ДНК код рака: поново посећена локација.Нат Рев Цлин Онцол.2018;15: 459-66.
19. КлеинЕА, Рицхардс Д, Цохн А, ТуммалаМ, Лапхам Р, Цосгрове Д, ет ал.Клиничка валидација циљаног теста за рано откривање вишеструких карцинома заснованог на метилацији коришћењем независног сета за валидацију.Анн Онцол.2021;32: 1167-77.
20. Ханахан Д, Веинберг РА.Карактеристике рака.Ћелија.2000;100: 57-70.
21. Ханахан Д. Ознаке рака: нове димензије.Цанцер Дисцов.2022;12: 31-46.
22. Сцхвартзберг Л, Ким ЕС, Лиу Д, Сцхраг Д. Прецизна онкологија: ко, како, шта, када, а када не?Ам Соц Цлин Онцол Едуц Боок.2017: 160-9.
23. Лиу Х, Менг Кс, Ванг Ј. Квантитативна метилација у реалном времену
откривање ПАКС1 гена у скринингу рака грлића материце.ИнтЈ Гинецол Цанцер.2020;30: 1488-92.
24. Империале ТФ, РансохоффДФ, Итзковитз СХ, Левин ТР, Лавин П, Лидгард ГП, ет ал.Мултитаргетстоол ДНК тестирање за скрининг колоректалног карцинома.Н ЕнглЈ Мед.2014;370: 1287-97.
25. Ли Ј, Ли И, Ли В, Луо Х, Кси И, Донг С, ет ал.Позиционирање водича
секвенцирање идентификује аберантне обрасце метилације ДНК који мењају ћелијски идентитет и мреже за надзор имуног тумора.Геном
Рес.2019;29: 270-80.
26. Гао К, ЛинИП, Ли БС, Ванг ГК, Донг ЛК, Схен БИ, ет ал.Ненаметљиво откривање више карцинома циркулишућим секвенцирањем ДНК метилације без ћелија (ТХУНДЕР): развој и независне студије валидације.Анн Онцол.2023;34: 486-95.
27. Донг С, Ли В, Ванг Л, Ху Ј, Сонг И, Зханг Б, ет ал.Гени повезани са хистонима су хиперметиловани код рака плућа и хиперметиловани
ХИСТ1Х4Ф би могао да послужи као биомаркер рака.Цанцер Рес.2019;79: 6101-12.
28. ХеијнсдијкЕА, Вевер ЕМ, АувиненА, Хугоссон Ј, Циатто С, Нелен В, ет ал.Ефекти скрининга антигена специфичног за простату на квалитет живота.Н ЕнглЈ Мед.2012;367: 595-605.
29. ЛузакА, Сцхнелл-Индерст П, Бухн С, Маиер-Зитароса А, Сиеберт У. Клиничка ефикасност тестова биомаркера за скрининг рака који се нуде као самоплаћајућа здравствена услуга: систематски преглед.Еур Ј Јавно здравље.2016;26: 498-505.
30. Донг С, Лу К, Ксу П, Цхен Л, Дуан Кс, Мао З, ет ал.
Хиперметиловани ПЦДХГБ7 као универзални само маркер рака и његова примена у раном скринингу рака грлића материце.Цлин Трансл Мед.2021;11: е457.
31. Иуан Ј, Мао З, Лу К, Ксу П, Ванг Ц, Ксу Кс, ет ал.Хиперметиловани ПЦДХГБ7 као биомаркер за рано откривање рака ендометријума у узорцима четкице ендометријума и стругањима грлића материце.Фронт Мол Биосци.2022;8: 774215.
32. Донг С, Ианг З, Ксу П, Зхенг В, Зханг Б, Фу Ф, ет ал.Узајамно
ексклузивна епигенетска модификација на СИКС6 са хиперметилацијом за праћење преканцерозног стадијума и појављивања метастаза.Сигнал Трансдуцт Таргет Тхер.2022;7: 208.
33. Хуанг Л, Гуо З, Ванг Ф, Фу Л. КРАС мутација: од нелековите до љековите код рака.Сигнал Трансдуцт Таргет Тхер.2021;6: 386.
34. Белински СА, Никула КЈ, ПалмисаноВА, МицхелсР, СаццоманноГ, ГабриелсонЕ, ет ал.Аберантна метилација п16 (ИНК4а) је рани догађај код рака плућа и потенцијални биомаркер за рану дијагнозу.Проц Натл Ацад Сци У СА.1998;95: 11891-6.
35. Робертсон КД.Метилација ДНК и људска болест.Нат Рев Генет.2005;6: 597-610.
36. ВентзенсенН, Валкер ЈЛ, Голд МА, Смитх КМ, ЗунаРЕ,
Матхевс Ц, ет ал.Вишеструке биопсије и откривање прекурсора рака грлића материце на колпоскопији.Ј Цлин Онцол.2015;33: 83-9.
37. Де Строопер ЛМ, Меијер ЦЈ, Беркхоф Ј, Хесселинк АТ, Снијдерс
ПЈ, Стеенберген РД, ет ал.Анализа метилације ФАМ19А4
ген у стругању грлића материце је веома ефикасан у откривању цервикса
карциноми и напредне ЦИН2/3 лезије.Цанцер Прев Рес (Пхила).2014;7: 1251-7.
38. Тхаи АА, Соломон БЈ, Секуист ЛВ, Гаинор ЈФ, Хеист РС.Рак плућа.Ланцет.2021;398: 535-54.
39. Груннет М, Соренсен ЈБ.Карциноембрионални антиген (ЦЕА) као туморски маркер код рака плућа.Рак плућа.2012;76: 138-43.
40. Воод ДЕ, КазероониЕА, Баум СЛ, ЕапенГА, ЕттингерДС, Хоу Л, ет ал.Скрининг карцинома плућа, верзија 3.2018, НЦЦН смернице за клиничку праксу у онкологији.Ј Натл Цомпр Цанц Нетв.2018;16: 412-41.
41. Америчко друштво за борбу против рака.Чињенице и бројке о раку.Атланта, Џорџија, САД: Америчко друштво за рак;2023. [ажурирано 1. марта 2023.;цитирано 2023. 22. августа].
42. ФонхамЕТХ, Волф АМД, Цхурцх ТР, ЕтзиониР, Фловерс ЦР,
Херциг А, ет ал.Скрининг рака грлића материце за појединце са просечним ризиком: ажуриране смернице за 2020. од Америчког друштва за рак.ЦА Цанцер Ј Цлин.2020;70: 321-46.
43. Цларке МА, Лонг БЈ, Дел Мар МориллоА, Арбин М, Баккум-Гамез ЈН, Вентзенсен Н. Повезаност ризика од рака ендометријума са крварењем у постменопаузи код жена: систематски преглед и мета-анализа.ЈАМА Интерн Мед.2018;178: 1210-22.
44. Јацобс И, Гентри-МахарајА, Бурнелл М, МанцхандаР, Сингх Н,
Схарма А, ет ал.Осетљивост трансвагиналног ултразвучног скрининга
за карцином ендометријума код жена у постменопаузи: студија случај-контрола унутар УКЦТОЦС кохорте.Ланцет Онцол.2011;12: 38-48.
45. БабјукМ, Бургер М, ЦомператеЕМ, Гонтеро П, МостафидАХ,
ПалоуЈ, ет ал.Смернице Европског удружења за урологију о неинвазивном карциному мокраћне бешике (ТаТ1 и карцином ин ситу) -
Ажурирање 2019.Еур Урол.2019;76: 639-57.
46. Арагон-Чинг ЈБ.Изазови и напредак у дијагностици, биологији и лечењу карцинома уротелног горњег тракта и бешике.Урол Онцол.2017;35: 462-4.
47. Ризви С, КханСА, Халлемеиер ЦЛ, Келлеи РК, Горес ГЈ.
Холангиокарцином – еволуирајући концепти и терапијске стратегије.Нат Рев Цлин Онцол.2018;15: 95-111.
48. Ие К, Линг С, Зхенг С, Ксу Кс. Течна биопсија у хепатоцелуларној
карцином: циркулишуће туморске ћелије и циркулишућа туморска ДНК.Мол Цанцер.2019;18: 114.
49. Зханг И, Иао И, Ксу И, Ли Л, Гонг И, Зханг К, ет ал.Пан-рак
откривање циркулишуће ДНК тумора код преко 10.000 кинеских пацијената.Нат Цоммун.2021;12: 11.
50. Еисенхауер ЕА, Тхерассе П, БогаертсЈ, Сцхвартз ЛХ, Саргент Д, Форд Р, ет ал.Нови критеријуми за евалуацију одговора код солидних тумора: ревидирана РЕЦИСТ смерница (верзија 1.1).Еур Ј Рак.2009;45: 228-47.
51. ЛитиереС, Цоллетте С, де Вриес ЕГ, Сеимоур Л, БогаертсЈ.РЕЦИСТ – учење из прошлости за изградњу будућности.Нат Рев Цлин Онцол.
2017;14: 187-92.
52. Сеимоур Л, БогаертсЈ, Перроне А, ФордР, Сцхвартз ЛХ, Мандрекар С, ет ал.иРЕЦИСТ: смернице за критеријуме одговора за употребу у испитивањима
тестирање имунотерапеутика.Ланцет Онцол.2017;18: е143-52.
53. ПантелК, Алик-Панабиерес Ц. Течна биопсија и минимална резидуална болест – најновија достигнућа и импликације за излечење.Нат Рев Цлин Онцол.2019;16: 409-24.
Цитирајте овај чланак као: Киан Ц, Зоу Кс, Ли В, Ли И, Иу В. Испостава против рака: само универзални маркери рака.Цанцер Биол Мед.2023;20: 806-815.
дои: 10.20892/ј.иссн.2095-3941.2023.0313
Време поста: 07.05.2024